A desigualdade na resposta ao tratamento de câncer
Uma das maiores frustrações na luta contra o câncer é a variação na eficácia dos tratamentos. A mesma terapia que salva uma vida pode falhar completamente em outra, deixando médicos e pacientes em busca de respostas. Agora, uma nova pesquisa publicada na renomada revista Nature Communications parece ter desvendado um dos motivos ocultos por trás dessa disparidade no tratamento de câncer.
Liderado pela Dra. Louise Fets no Laboratório de Ciências Médicas (LMS) do Medical Research Council (MRC), o estudo revela que a forma como as drogas se distribuem dentro das células tumorais é crucial, e pequenas estruturas celulares, conhecidas como lisossomos, desempenham um papel inesperado nesse processo.
O desafio da eficácia no tratamento de câncer
Nos últimos anos, as opções de tratamento de câncer se expandiram significativamente, trazendo esperança e melhorando os resultados para muitos. Os inibidores de PARP, por exemplo, revolucionaram o cuidado de câncer de ovário, de mama e de próstata. No entanto, nem todos os pacientes se beneficiam, e alguns desenvolvem resistência ao longo do tempo, um obstáculo persistente na oncologia.
Para que esses medicamentos funcionem, eles precisam atingir e se acumular dentro das células cancerosas em níveis suficientes para induzir a morte celular. Apesar disso, a ciência ainda tem uma compreensão limitada de como as drogas se distribuem dentro dos tumores e quais mecanismos controlam esse processo vital. A pesquisa recente aponta que a eficácia não depende apenas de a droga alcançar o tumor, mas de como ela se espalha internamente.
Essa lacuna no conhecimento tem sido um dos grandes entraves para otimizar as terapias existentes e desenvolver novas abordagens mais eficazes. Compreender a dinâmica interna das drogas é fundamental para superar a resistência e garantir que o tratamento de câncer seja o mais potente possível para cada indivíduo.
Mapeando a jornada das drogas dentro dos tumores
Para investigar a distribuição das drogas, os pesquisadores utilizaram uma abordagem inovadora. Eles trabalharam com fatias finas de tumores ovarianos de pacientes, mantidas vivas em laboratório – os chamados “explantes”. Esses tecidos foram tratados com inibidores de PARP, permitindo que os cientistas observassem diretamente como os medicamentos se moviam através do tecido tumoral humano real.
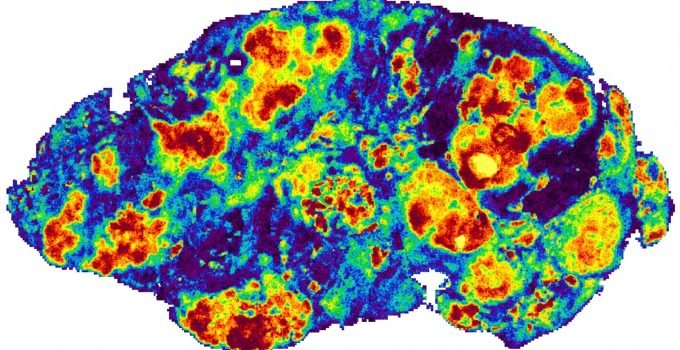
Com o auxílio da imagem por espectrometria de massa, a equipe produziu mapas detalhados que mostravam exatamente onde as drogas se acumulavam. Essa técnica foi combinada com a transcriptômica espacial, que permitiu examinar a atividade genética em áreas com altos e baixos níveis de drogas dentro da mesma amostra. Os resultados foram surpreendentes e revelaram diferenças marcantes na distribuição dos medicamentos, tanto dentro de tumores individuais quanto entre diferentes pacientes, mesmo quando a mesma dose era administrada.
A Dra. Zoe Hall, autora sênior do estudo, destacou a importância dessa metodologia: “Um aspecto inovador deste estudo foi o uso da imagem por espectrometria de massa para medir e visualizar diretamente a captação de drogas no tecido tumoral do paciente. Através do mapeamento espacial das moléculas de drogas, pudemos identificar regiões de alta e baixa concentração e comparar a expressão gênica da mesma fatia de tecido, usando transcriptômica espacial.”
Lisossomos: os reservatórios ocultos de medicamentos
A grande revelação do estudo foi o papel central dos lisossomos nessa distribuição desigual. Os pesquisadores descobriram que alguns inibidores de PARP são atraídos para esses compartimentos celulares, que funcionam como “centros de reciclagem” da célula, e são armazenados lá em vez de se espalharem uniformemente. Isso cria “bolsões” internos onde as drogas se acumulam de forma concentrada.
Esses lisossomos atuam como reservatórios de liberação lenta, retendo a droga e liberando-a gradualmente. Esse mecanismo aumenta a exposição de certas células ao tratamento, enquanto outras recebem níveis muito mais baixos, comprometendo a eficácia geral. A Dra. Carmen Ramirez Moncayo, primeira autora do estudo, expressou surpresa: “Ficamos surpresos ao ver uma grande variabilidade na acumulação de drogas no nível de célula única. Essa variabilidade foi impulsionada pelo acúmulo de uma droga em lisossomos, que estão agindo como reservatórios, aumentando a exposição das células cancerosas a drogas, armazenando e liberando a droga quando necessário.”
É importante notar que nem todos os inibidores de PARP se comportam da mesma maneira. O estudo observou que medicamentos como rucaparib e niraparib são afetados por esse processo, enquanto outros, como o olaparib, não são. Essa diferenciação é crucial para entender como otimizar o tratamento de câncer e escolher a droga mais adequada para cada perfil tumoral.
Implicações para o futuro da medicina oncológica
Os inibidores de PARP já são amplamente utilizados no tratamento de câncer de ovário, mama e próstata, e estão sendo testados em muitos outros tipos de câncer. Obter uma compreensão mais aprofundada de como esses medicamentos são armazenados e distribuídos dentro das células pode levar a estratégias de tratamento mais personalizadas, aumentando a eficácia e reduzindo a resistência e a recidiva.
A Dra. Louise Fets, autora sênior, enfatiza o potencial dessa descoberta: “Ao entender como as drogas são absorvidas pelas células, podemos entender se isso influencia por que os medicamentos contra o câncer funcionam para algumas pessoas e não para outras. Eventualmente, esperamos ser capazes de estudar a assinatura molecular do tumor de um paciente para ajudar a adaptar as abordagens terapêuticas de uma forma mais personalizada.”
Embora este estudo tenha sido realizado com tecido tumoral mantido fora do corpo, e em pacientes reais a entrega das drogas é feita através da corrente sanguínea (onde os vasos tumorais são muitas vezes desorganizados, contribuindo para uma distribuição ainda mais desigual), os próximos passos incluem estudos em modelos animais e grupos maiores de pacientes. O objetivo é compreender melhor a interação entre a entrega da droga, a estrutura do tumor e o armazenamento lisossomal em contextos clínicos, incluindo casos de câncer recidivado, pavimentando o caminho para um tratamento de câncer mais inteligente e direcionado.